Ambos os isômeros têm exatamente os mesmos átomos na mesma ordem. Isto significa que as forças de dispersão entre as moléculas de van der Waals serão as mesmas em ambos os casos. A diferença entre os dois é que o isômero cis é uma molécula polar, enquanto o isômero trans é apolar.
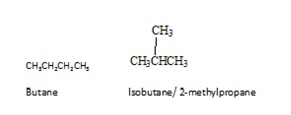
Isômeros são compostos diferentes com a mesma fórmula molecular. Existem diferentes tipos de isômeros. Os isômeros podem ser divididos principalmente em dois grupos: isômeros constitucionais e estereoisômeros. Isômeros constitucionais são isômeros nos quais a conectividade dos átomos difere nas moléculas. Butano é o alcano mais simples que apresenta isomeria constitucional. O butano possui dois isômeros constitucionais, o próprio butano e o isobuteno.
Nos estereoisômeros, os átomos estão conectados na mesma sequência, ao contrário dos isômeros constitucionais. Os estereoisômeros diferem apenas na disposição de seus átomos no espaço. Os estereoisómeros podem ser de dois tipos, enantiómeros e diastereómeros. Diastereômeros são estereoisômeros cujas moléculas não são imagens espelhadas umas das outras. Os isômeros cis trans de 1,2-dicloroetano são diastereômeros. Enantiômeros são estereoisômeros cujas moléculas são imagens espelhadas não sobreponíveis umas das outras. Os enantiômeros aparecem apenas com moléculas quirais. Uma molécula quiral é definida como aquela que não é idêntica à sua imagem espelhada. Portanto, a molécula quiral e sua imagem espelhada são enantiômeros uma da outra. Por exemplo, a molécula de 2-butanol é quiral e sua imagem e seu espelho são enantioméricos.
Como mencionado acima, o isomerismo cis trans ou, em outras palavras, o isomerismo E-Z é uma forma de estereoisomeria. O sistema de transcrição Cis é aplicado para nomear compostos simples, enquanto o sistema E-Z é usado para moléculas mais complicadas. Quando uma molécula tem rotação restrita em um sítio específico, os isômeros cis e trans podem existir.
Quando há ligações duplas carbono-carbono, há uma rotação estreita, de modo que pode haver isômeros trans cis. Numa molécula como o 1,2-dibromoeteno, dois grupos bromo podem estar no mesmo lado da ligação dupla ou no lado oposto da ligação dupla. Isso não importa se a ligação for uma ligação simples, porque então os átomos podem girar. Porém, neste caso, duas moléculas não são iguais. Embora os isômeros Cis e trans tenham a mesma fórmula molecular e peso molecular, suas propriedades físicas são diferentes.
